Bakterielle infeksjoner som ikke lar seg behandle på grunn av antibakteriell resistens er en akutt og økende global utfordring. På verdensbasis er det mer enn 700 000 mennesker som dør årlig som følge av infeksjoner forårsaket av antibiotika-resistente bakterier.
I en rapport fra 2018 la FN frem et worst-case scenario der vi kan komme i en situasjon der slike infeksjoner kan ta 10 millioner liv årlig dersom det ikke gjøres tiltak. Siden dagens antibiotika raskt er i ferd med å bli mindre effektive og utvikling av nye antibiotika er svært tidkrevende, er det et stort og umiddelbart behov for nye løsninger.
Et kinderegg mot antibiotikaresistens
Det treårige forskerprosjektet «Graphene-based drug delivery systems for treating MRSA infections» (GraMI) ble tildelt 15 MSEK av NordForsk i januar 2021, og vil fokusere på behandling av methicilin-resistant Staphylococcus Aureus (MRSA) – tidligere noe misvisende kalt «sykehusbakterier» – som blant annet forårsaker kroniske hudinfeksjoner og blodforgiftning (sepsis). MRSA kan også infisere vev og organer i kroppen, som for eksempel hjerte og lunger, og kan trives og vokse på ulike typer implantater brukt i helsevesenet. MRSA-infeksjoner spres svært lett på sykehus, og er svært belastende og farlig for pasientene som rammes.
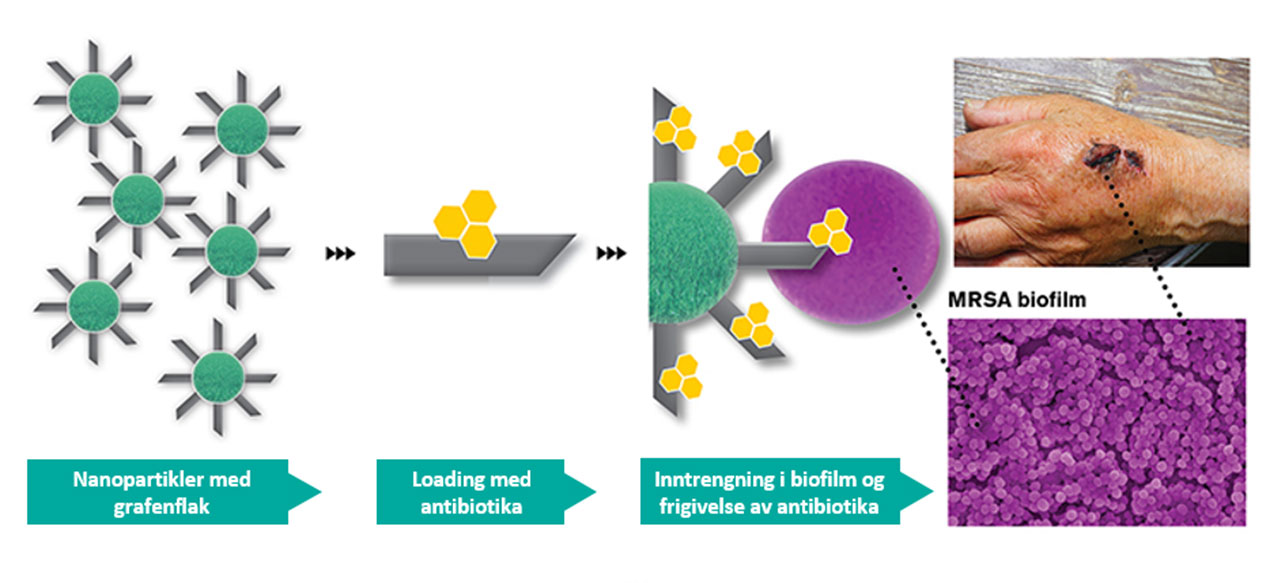
Ideen bak GraMI er å kombinere tre allerede etablerte metoder – antibiotika, metalliske nanopartikler og grafenflak – på en helt ny måte for å lage en ny teknologi for levering av legemidler, som vist i figuren under. Alle de tre metodene har antibakterielle egenskaper hver for seg, og i kombinasjon vil de kunne være enda mer effektive, siden disse partiklene mest sannsynlig kan trenge seg inn i den bakterielle biofilmen på overflaten av infeksjonen og frigi antibiotikaen der. Biofilm er det tykke, beskyttende laget av bakterier og slim (mucus) som dannes når bakteriene binder seg til en overflate og starter å formere seg. De skarpe grafenflakene kan skjære seg gjennom den beskyttende biofilmen og kan levere antibiotikaen direkte til det infiserte området.
Oversikt over den bærende ideen i GraMI (modifisert etter avtale fra Chalmers artikkel)
Chalmers i Göteborg er ett av de verdensledende universitetene innenfor forskning på grafen. Ideen med å bruke grafen til medisinsk behandling er relativt ny, og innebærer mange nye muligheter. Forskningsgruppen til professor August Yurgens ved Institutt for Mikroteknologi og Nanovitenskap utvikler en prosess der nanopartikler dekkes av grafenflak som vist i figuren. Professor Yurgens og gruppen hans har allerede vist at de skarpe kantene på grafenflak som stikker vertikalt ut fra en overflate kan skjære seg gjennom membraner på celler av en bestemt størrelse. Nærmere bestemt skjærer grafenflakene seg gjennom små, bakterielle celler, mens større celler, som dem man finner i mennesker, ikke skades. En vanlig utfordring med bruk av antibiotika er at det ikke trenger tilstrekkelig dypt inn i biofilmen. I GraMI vil dette bli løst ved at antibiotikaen bindes til grafenflakene som skjærer seg gjennom biofilmen og leverer antibiotikaen gradvis inne i det infiserte vevet.
Grønne nanopartikler og nye antibiotika
Partneren fra Danmarks Tekniske Universitet (DTU) skal produsere såkalte grønne metalliske nanopartikler, som fremstilles ved hjelp av ekstrakter fra planter eller bakterier for en mer miljøvennlig produksjon. Disse vil bli benyttet som stillasverk for grafenflakene. Siden de grønne nanopartiklene er sfæriske, vil det være en utfordring å oppnå jevn og kontrollerbar belegning av nanopartiklene med grafenflak som vist i figuren.
Prosjektteamet ved SINTEF, ledet av Dr. Andreas Åslund, vil bidra med sin erfaring innenfor utvikling av nye antibiotika, metalliske nanopartikler, funksjonalisering av grafenflak og andre nanostrukturer, og formulering av aktive ingredienser. SINTEF har lang erfaring med å identifisere og utvikle teknologi for nye antibiotika, for eksempel fra bakterier fra havet, og å utvikle nanoformuleringer basert på kjente og nye antibiotika (for eksempel via prosjektet NAREB – Nanotherapeutics for Antibiotic Resistant Emerging Bacterial Pathogens). GraMI inngår i den strategiske nanomedisinsatsningen i SINTEF, som omfatter et bredt spenn fra utvikling av nye partikkelsystemer til innkapsling av legemidler og karakterisering av disse nanomedisinene fysisk, kjemisk, i celler (in vitro) og i dyr (in vivo). Å bruke nanomedisin i prosjekter mot infeksjonssykdommer er ett av satsningsområder innenfor nanomedisin SINTEF har jobbet målrettet mot.
Mekanismer som effektivt kan benyttes mot MRSA
Professor Ivan Mijakovic og forskningsgruppen hans vil undersøke hvor godt de nye nanopartiklene fungerer – eller mer spesifikt, i hvor stor grad de kan drepe bakterielle biofilmer. Grafenbasert nanoteknologi er ennå ikke tillatt i medisinsk behandling i EU, men det er flere kliniske forsøk som pågår for å sikre at behandlingsformen er tilstrekkelig trygg. Det tar vanligvis flere tiår å utvikle behandlingsformer som foreslått i GraMI, men ifølge Professor Mijakovic representerer GraMI-teamet forskningsfronten med tanke på å utvikle en ny mekanisme vi tror kan benyttes effektivt mot MRSA og andre farlige patogener. Derfor er det viktig at vi handler nå og tester disse nye systemene så fort som mulig.









Kommentarer
Ingen kommentarer enda. Vær den første til å kommentere!