Ved hjelp av ny elektrolyseteknologi kan industrielle avfallsstrømmer bli en «gullgruve» for det kritiske råmaterialet mangan.
Mangan (Mn) er et avgjørende materiale for det grønne skiftet og en essensiell ingrediens i mange teknologier og produkter. Blant annet finner vi mangan(oksid) i kombinasjon med nikkel- og koboltoksid i katodematerialet i litium-ion-batterier. Metallisk mangan brukes hovedsakelig i stål, men også i legering med andre metaller slik som aluminium. Råmaterialet for å produsere metallisk mangan er enten malm, hentet fra gruvedrift, eller det kan fremstilles fra sekundære kilder, slik som ved resirkulering og utnytting av industrielle avfallsstrømmer.
Utnytting av sekundære kilder vil bidra til å redusere produktenes miljøavtrykk, gjøre prosessen mer sirkulær og minske forsyningsrisikoen. Og her er potensialet stort: Gjennomsnittstall fra 2007 til 2010 viser at mer enn 20 000 tonn slam som inneholder mangan fra manganlegeringsindustrien deponeres i Norge hvert år. Her avgis slam som biprodukt etter at avgasser fra ovnene renses og skrubbes. Slammet, som består av vann, støvpartikler og andre avgasskomponenter, inneholder også typisk mellom 20-30 % verdifullt mangan.

En annen viktig industriell avfallsstrøm er avfall fra sinkmetallproduksjon. Her felles det kontinuerlig ut mangandioksid på anoden i elektrolyseprosessen. Dette «anodeskallet» bygger seg opp over tid og må fjernes med jevne mellomrom for at sinkelektrolysen skal fungere best mulig.
Elektrolyseteknologi gir rene manganprodukter
Mesteparten av det metalliske manganet som lages er legert med andre metaller som jern og silisium og brukes videre til stålproduksjon. Slikt metallisk mangan produseres i smelteprosesser, der en ikke trenger å separere manganet fra øvrige metaller. For å få helt rent manganmetall, uten legeringselementer, må en bruke elektrolyse. Dette kalles også elektrolytisk manganmetall (EMM). EMM brukes til å produsere mangan til blant annet aluminiumslegeringer, elektronikk og kjemikalier, men i dag produserer Kina mer enn 95 prosent (kilde: RMIS – Raw materials information system (EU)
Ved elektrolyse kan en også produsere elektrolytisk mangandioksid (EMD). EMD er mye brukt i alkaliske batterier som anvendes i alt fra fjernkontroller, radioer, kalkulatorer, klokker, kameraer med mere.
«To fluer i en smekk»
Elektrolytisk produksjon av manganmetall og mangandioksid foregår i dag i to separate prosesser. Gjennom et SINTEF-støttet prosjekt har forskerne kommet frem til hvordan de kan kombinere disse to produksjonsmetodene til én enkelt elektrolytisk prosess. Prosessen gjør det mulig å produsere et ekstra verdifullt produkt til omtrent samme energikostnad. Mer konkret vil en ved å produsere 1 kg manganmetall samtidig også produsere 2,5 kg mangandioksid, uten at det går ut over energibruken, det vil si til sammen 7-8 kWh.
Å lage to separate produkter fra samme råmateriale i én enkelt prosess vil redusere kostnader, energiforbruket, samtidig som mengden avfall som trenger spesiell behandling eller deponering minskes.
Med andre ord vil verdifullt «slam» fra industrielle avfallsstrømmer slik kunne utnyttes på en kostnadseffektiv og bærekraftig måte.
Manganproduksjon på katoden og mangandioksid på anoden
I den kombinerte elektrolytiske prosessen, dannes mangandioksid på anoden, mens manganmetall dannes på katoden. For å oppnå best mulig kvalitet på produktene og ha et så lavt energiforbruk som mulig, må det benyttes to forskjellige elektrolytter: én til å lage manganmetall (katolytt) og én for å lage mangandioksid (anolytt). For å holde katolytten og anolytten adskilt, ble det benyttet en membran mellom anoden og katoden.
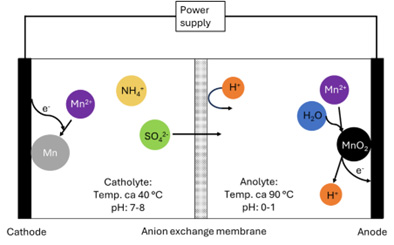
Krever ulike elektrolytiske forhold
Manganmetall er veldig uedelt, derfor vil det alltid foregå noe hydrogenutvikling på katoden samtidig som metallet felles ut, og dette «stjeler» energi. Ved produksjon av manganmetall må elektrolyttsammensetningen derfor optimaliseres for at hydrogenproduksjonen skal bli så liten som mulig. For å få til dette så bør pH i katolytten være så høy som mulig (pH 7-8), men samtidig ikke så høy at mangan-ionene feller ut som manganhydroksid og dermed reduserer mengden råmateriale tilgjengelig for å produsere metallet. Over tid vil hydrogenutviklingen imidlertid føre til at pH øker. Derfor tilsettes det en buffer, for å forhindre at pH blir for høy. Temperaturen er også en viktig faktor for energiforbruket, for å oppnå en så jevn metalloverflate som mulig og unngå kortslutning i cellen. Temperaturer rundt 40 grader blir derfor bruk.
Ved produksjon av mangandioksid av høy kvalitet må pH i elektrolytten, i motsetning til ved produksjon av manganmetall, være lav (pH 0-1). Temperaturen i anolytten er også forskjellig fra katolytten. Her er optimal temperatur rundt 90 grader.
For å få til de to ulike temperaturene i samme prosess har vi i prosjektet adskilt anolytten og katolytten i hver sin beholder med riktig temperatur, samtidig som anolytten og katolytten kontinuerlig sirkuleres mellom beholderne og cellen hvor utfellingen av metall og mangandioksid foregår.
Ved å dra nytte av ny elektrolyseteknologi og den store mengden mangan som finnes i industrielle avfallsstrømmer, kan avfall gjøres om til verdifulle produkter og bidra til en grønnere og mer sirkulær industri. Den nye prosessen vil i tillegg bidra til viktige energibesparelser for samfunnet og miljøet.













Kommentarer
Ingen kommentarer enda. Vær den første til å kommentere!